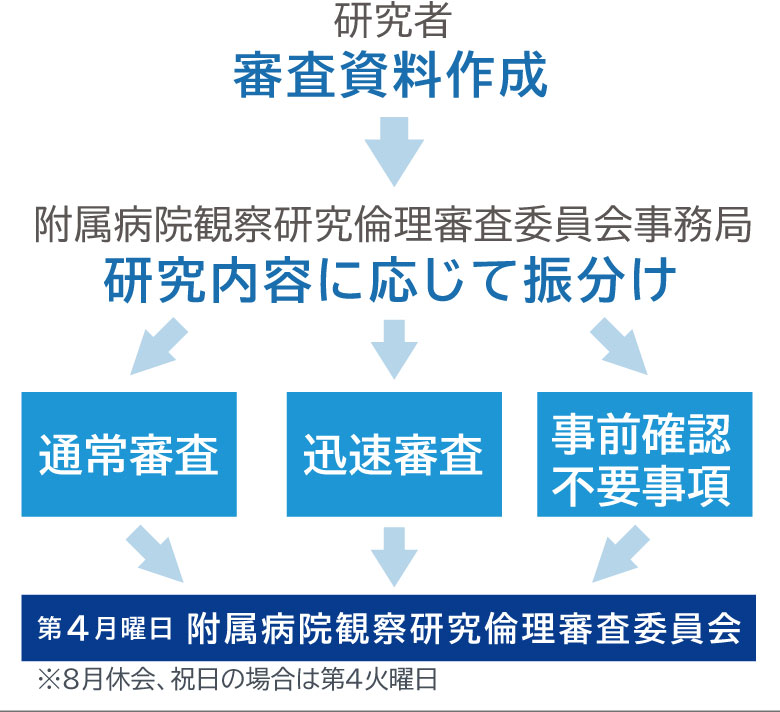
附属病院観察研究倫理審査委員会(侵襲なし・遺伝子情報を扱わない)
当院の患者さんを対象または当院施設を利用した観察研究の審議を目的として、2022年10月より附属病院観察研究倫理審査委員会が設置されました。遺伝子情報を扱わない観察研究を中心に審議しています。
開催日程
- :
毎月第4月曜日午後2 時~(8月休会、祝日の場合は第4火曜日開催)
病院3階セミナー室1にて開催 - 提出・問い合わせ先
- :附属病院観察研究倫理審査委員会事務局
- 提出方法
- :メールで送信(一部書類は学内便で提出。メール受領後に案内いたします。)
- メールアドレス
- :hsp-kansaturinri [at] chiba-u.jp
申請の流れ(手続きフロー)
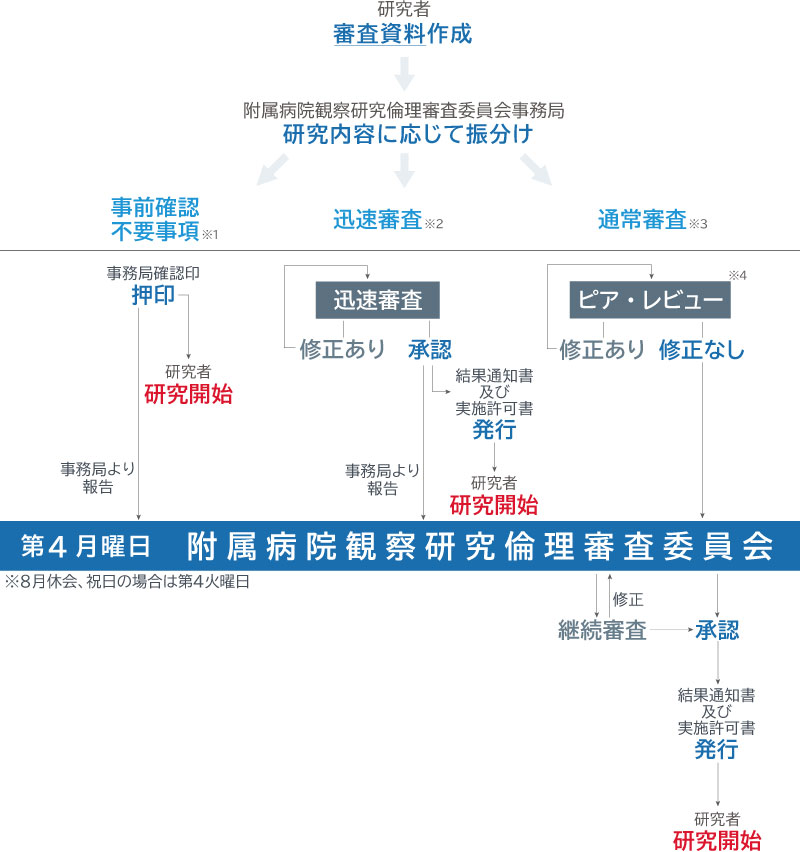
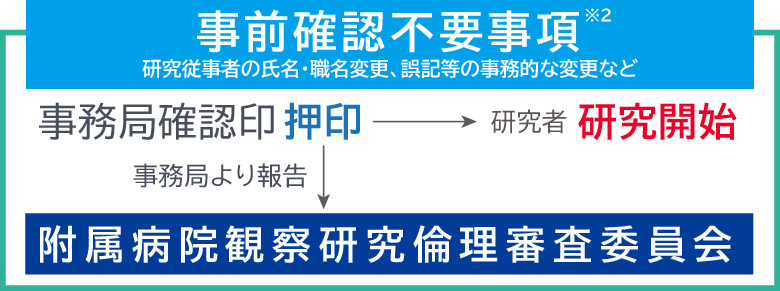
- ※1
- 事前確認不要事項:研究従事者の氏名・職名変更、誤記等の事務的な変更など
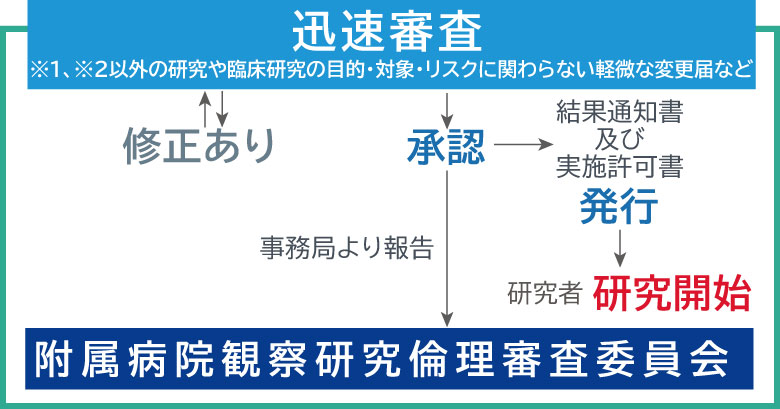
- ※2
- 迅速審査:※1、※3以外の研究や臨床研究の目的・対象・リスクに関わらない軽微な変更届など
- ※3
- 通常審査:介入を行うものや委員会での審議が必要な場合など
- ※4
- ピア・レビュー:各診療科の品質管理専門委員から選出されたレビュアーによる書類チェック
附属病院観察研究倫理審査委員会への提出書類
下記書類のうち必須書類および必要に応じてその他の書類をご作成いただき、観察研究倫理審査委員会事務局にメールにてご提出ください。※2023年1月より受付開始いたします。
提出書類等、申請に関してご不明点があれば相談フォームからお問い合わせください。
新規申請
| 様式・テンプレート | 千葉大学 のみで実施 |
多機関共同研究 | ||
|---|---|---|---|---|
| 個別審査 | 千葉大学主導千葉大学で 一括審査 手続き方法 |
他機関主導 他機関で 一括審査 手続き方法 |
||
| 様式1 申請書 | ◎ |
◎ |
◎ |
|
| 研究計画書 | ◎ |
◎ |
◎ |
|
| 説明文書・同意書 ※1 | ○ |
○ |
○ |
|
| 情報公開文書 ※2 | ○ |
○ |
○ |
|
| アセント文書 ※3 | ○ |
○ |
○ |
|
| 利益相反に関する 自己申告書 |
◎ |
◎ |
◎ |
|
| 関与する組織及び試料・情報の流れを記載した図(任意様式) | ◎ |
◎ |
◎ |
|
| 様式1 別紙1 研究者一覧 |
◎ |
◎ |
◎ |
|
| 様式1 別紙2 研究機関要件確認書 |
|
|
◎ |
|
| 様式1 別紙3 研究実施体制 |
|
◎ |
◎ |
|
| 主たる研究機関の 承認通知等 |
|
◎ |
|
|
| 先行研究の 説明文書・同意書 |
△ |
△ |
△ |
|
| 先行研究の 倫理委員会承認通知 ※4 |
△ |
△ |
△ |
|
|
【その他】 アンケートやポスターなどを使用した研究を行う場合、 アンケート用紙やリクルート資料など研究に必要とされる書類は適宜提出 |
||||
- ◎
- …… 必須書類
- ○
- …… 必要に応じてご提出ください。
- △
- …… 過去に行われた研究で収集した試料・情報を利用・提供する場合、先行研究の説明文書・同意書、
倫理審査の委員会承認通知も併せてご提出ください。
- ※1
- …… 文書同意、オプトアウトなどの要否・適用条件についてはこちらをご覧ください。
- ※2
- …… 記載すべき内容としては生命科学・医学系指針(第4章第8の第6項、研究対象者等に通知し、
又は研究対象者が容易に知り得る状態におくべき事項)を参照してください。
- ※3
- …… インフォームド・アセントを得る場合の手続等は、生命科学・医学系指針(第4章第9の第2項、インフォームド・アセントを得る場合の手続き等)を参照してください。
アセント文書を作成する場合には、下記の小児治験ネットワークCRC部会にて作成されたアセント文書雛型等を参考にしてください。なお、公開されている雛型は治験用なので、計画内容に合わせて適宜修正してください。
小児治験ネットワーク
- ※4
- …… 先行研究が千葉大学の倫理審査委員会で承認されている場合、提出不要となる場合もあります。
詳しくはこちらの文書を参照してください。
【参考】
・人を対象とする生命科学・医学系研究に関する倫理指針 令和3年3月23日(令和5年3月27日一部改正)
・ガイダンス 令和3年4月16日(令和6年4月1日一部改訂)
変更申請
承認された研究の実施中に研究計画書の内容を変更する場合に提出が必要となります。本様式に加えて、初回の倫理審査委員会に提出した書類に変更がある場合は、 変更部分に黄色ハイライトをつけてご提出ください。
2023年1月より前に医学研究院倫理審査委員会で承認された研究課題の変更申請は、これまでどおり医学研究院倫理審査委員会に申請してください。(医学研究院倫理審査委員会サイトはこちら)
定期報告
研究開始より定期的に施設長に対して研究の実施状況を報告してください。倫理審査委員会事務局より、提出に必要な様式と共に案内するので、それに従い書類を作成、ご提出ください。
附属病院観察研究倫理審査委員名簿
議事録公開
過去の議事録は、厚生労働省の倫理審査委員会報告システムで公開しています。