臨床研究利益相反管理委員会
臨床研究に関する利益相反の審議を行う体制の整備
臨床研究は、人を対象とした研究であることから、研究対象者の安全性の確保や権利・利益の保護を最優先に考えて研究を実施していくことが求められます。研究の信頼性を確保するため、臨床研究を行う研究者は、ヘルシンキ宣言などの倫理原則および各種規制要件に基づき、資金提供、スポンサー、研究関連組織との関わり、その他起こり得る利益の衝突、研究対象者に対する謝礼等について、開示する責務があります。
臨床研究利益相反管理委員会では、「臨床研究に係る利益相反自己申告書」により審議を行い、利益相反の管理を行っています。
臨床研究の種類、内容によって、提出することになっている書式が異なりますので、必要な書式については、「書類ダウンロード」ページからご確認ください。
Conflict of Interest:COI
利害の対立、利害の衝突、利益相反について
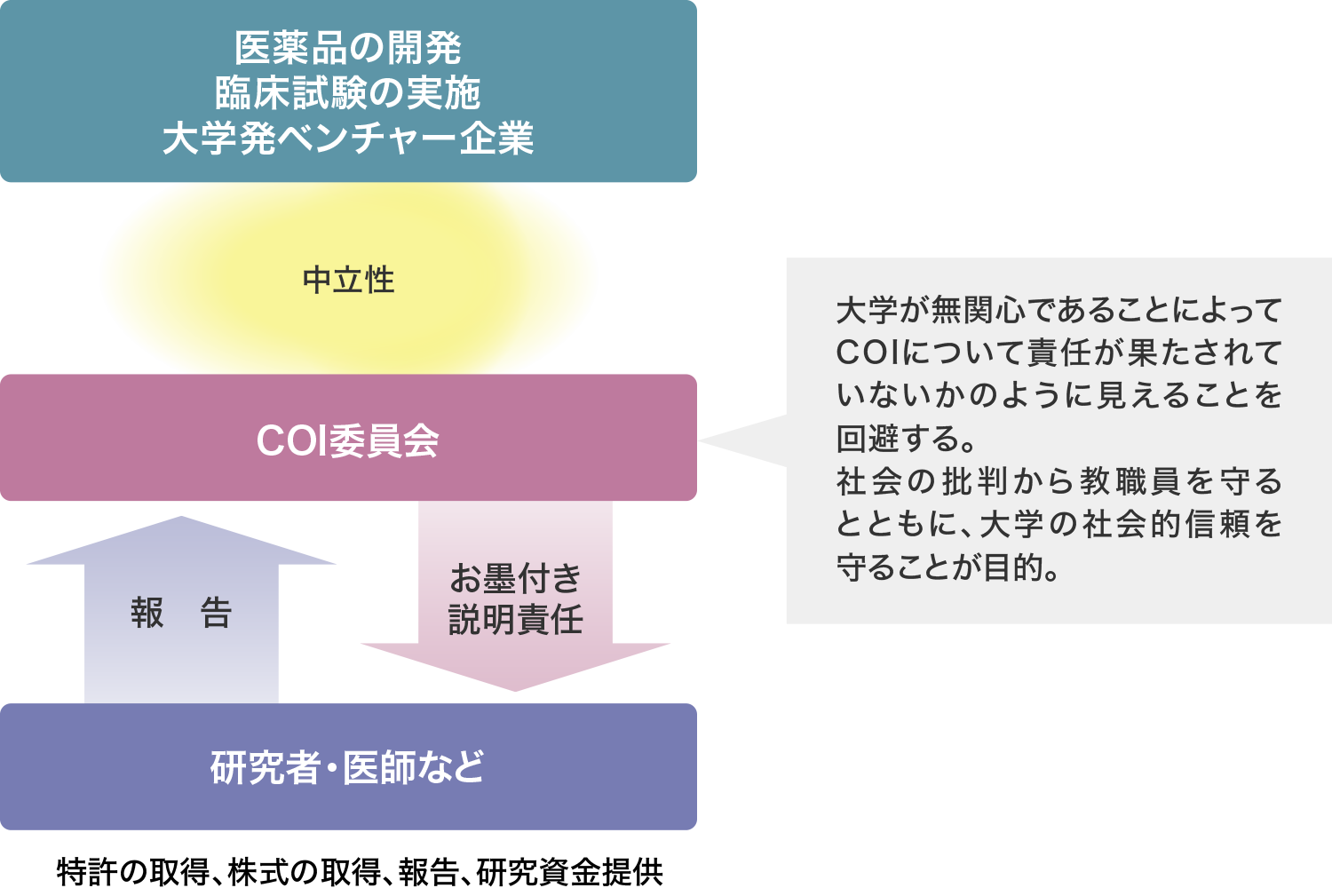
臨床研究における「利益相反」とは、臨床研究の実施にあたり、臨床研究実施者等の研究の実施並びに研究対象者及び被験者の人権・生命・安全の保護に対する責任と、当該臨床研究実施者等が個人的に得る経済的又は社会的利益(研究資金提供、報酬、株式の取得など)とが衝突・相反する状態をいいます。